|
济宁医疗器械注册检验范围和项目简析时间:2022-09-22 1. 注册检测范围 注册检测是在CFDA认可的检测机构,按照企业自行编制的产品技术要求(产品注册标准)对产品样品的性能指标及随附的产品说明书、标签等进行符合性核查的一个过程。 对于第II、III类医疗器械产品,注册前必须要在经CFDA认可的检测机构取得检测报告,并将检测报告作为注册申请的主要资料之一提交给CFDA进行审查;对于I类医疗器械,备案时可提交企业自测报告或第三方测试报告。 2. 注册检测服务
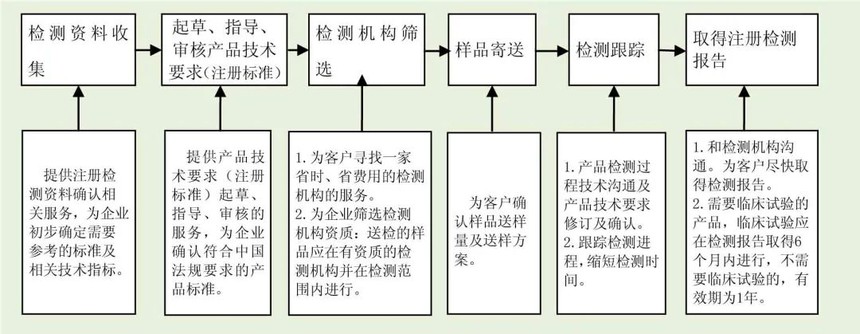
3.服务流程
4. 常规检测项目
备注:
|